Laboratorium Analiz Biologicznych
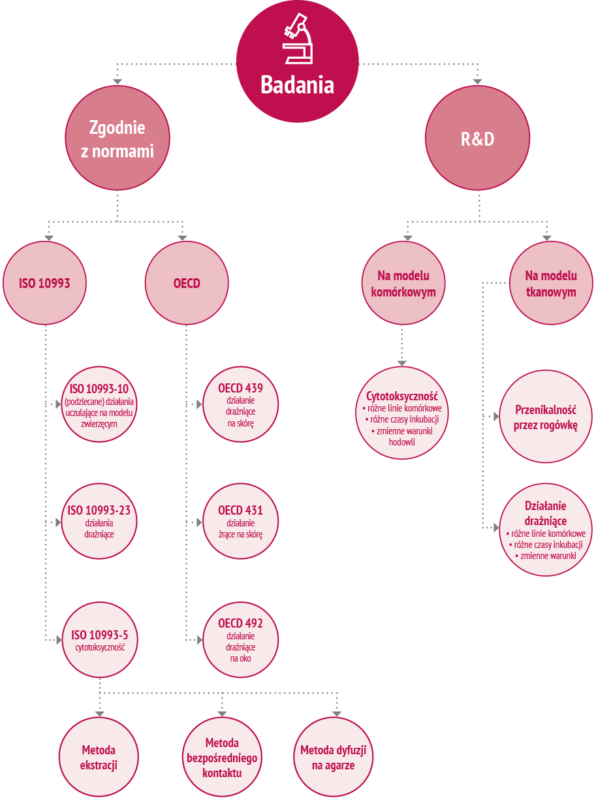
Badania wyrobów medycznych
Cytotoksyczność in-vitro ilościowa, metodą wychwytu czerwieni obojętnej (NRU) wg ISO 10993-5
Test cytotoksyczności ma na celu ocenę ogólnej toksyczności wyrobów i materiałów medycznych. Badanie polega na ekstrakcji wyrobów i materiałów medycznych w pożywce hodowlanej (zgodnie z ISO 10993-12) w określonych warunkach temperatury i czasu. Następnie przygotowywany jest szereg ośmiu rozcieńczeń ekstraktu i wystawienie na jego działanie przez określony czas mysich fibroblastów (linia Balb3t3/L929 ) w 6 powtórzeniach. Ocena działania cytotoksycznego jest wykonywana metodą ilościową za pomocą testu wychwytu czerwieni obojętnej (NRU) lub testu MTT. Test NRU pozwala zmierzyć ilość wychwyconego barwnika po ekspozycji komórek na badaną substancję, który akumuluje się w lizosomach komórek żywych, natomiast test MTT umożliwia pomiar aktywności enzymów mitochondrialnych w komórce, co jest wprost proporcjonalne do ilości zredukowanej soli tetrazolowej, a tym samym może być wyznacznikiem żywotności komórek.
Badanie drażliwości/drażnienia skóry in-vitro za pomocą modelu rekonstruowanego naskórka ludzkiego (RHE) wg ISO 10993-23
Test podrażnienia skóry in-vitro służy do przewidywania ostrego podrażnienia skóry przez wyroby medyczne. Badanie polega na ekstrakcji wyrobów i materiałów medycznych w soli fizjologicznej oraz oleju sezamowym (zgodnie z ISO10993-12), a następnie wystawieniu na działanie ekstraktu przez określony czas rekonstruowanego ludzkiego naskórka – RHE SkinEthic. Efekt podrażnienia objawia się poprzez wzrost efektu cytotoksyczności ekstraktów na RHE, który jest mierzony ilościowo za pomocą testu MTT. Test MTT umożliwia pomiar aktywności enzymów mitochondrialnych w komórce, co jest wprost proporcjonalne do ilości zredukowanej soli tetrazolowej, a tym samym może być wyznacznikiem żywotności komórek – RHE SkinEthic i/lub równoważny.
Uwaga! W JCI nie prowadzimy badań implantów (wyrobów medycznych implantowanych)
Badania na komórkach
- Cytotoksyczność za pomocą testu MTT, NRU i oznaczanie IC50
- Badanie żywotności komórek w czasie
- Badanie stresu oksydacyjnego
- Badanie wydzielania czynników wzrostu
Badania na rekonstruowanych ludzkich tkankach
- Działanie drażniące i/lub żrące na skórę/oko – test wykorzystujący rekonstruowane ludzkie tkanki (EpiDerm™, EpiOcular™) w warunkach in-vitro, który służy jako badanie oceny zagrożenia (hazard assessment) do przewidywania ostrego podrażnienia skóry lub oka przez substancję lub mieszaninę. Polega na zaaplikowaniu badanej próbki bezpośrednio na tkankę a następnie poddanie jej działaniu przez określony czas. Efekt podrażnienia objawia się poprzez wzrost efektu cytotoksyczności, który jest mierzony ilościowo za pomocą testu MTT. Test MTT umożliwia pomiar aktywności enzymów mitochondrialnych w komórce, co jest wprost proporcjonalne do ilości zredukowanej soli tetrazolowej, a tym samym może być wyznacznikiem żywotności komórek.
- Stopień podrażnienia skóry/oka – test wykorzystujący rekonstruowane ludzkie tkanki (EpiDerm™, EpiOcular™) w warunkach in-vitro, który służy jako badanie przesiewowe w celu oceny ryzyka (risk assessment) w celu przypisania oczekiwanego działania drażniącego na podstawie wyników czasu pojawienia się efektu toksycznego. Badanie jest również stosowane do uszeregowania testowanych preparatów według ich potencjału drażniącego skóry lub oka.
Badanie działania drażniącego na skórę za pomocą modelu rekonstruowanego naskórka ludzkiego (RHE) zgodnie z OECD 439
Badanie przeznaczone jest dla wszystkich substancji, które podlegają rejestracji zgodnie z Rozporządzeniem REACH. Pozwala na rozróżnienie i zaklasyfikowanie badanej substancji jako „nie drażniącej” co odpowiada „No Category” wg GHS lub „drażniącej” co odpowiada połączonej „Category 1” razem z „Category 2” wg GHS.
Badanie działania żrącego na skórę za pomocą modelu rekonstruowanego naskórka ludzkiego (RHE) zgodnie z OECD 431
Badanie przeznaczone jest dla wszystkich substancji, które podlegają rejestracji zgodnie z Rozporządzeniem REACH. Pozwala na rozróżnienie i zaklasyfikowanie badanej substancji jako „drażniącej” co odpowiada „Category 1” wg GHS lub „żrącej” co odpowiada „Category 2” wg GHS.
Badanie działania drażniącego na oko za pomocą modelu rekonstruowanego ludzkiego nabłonka oka zgodnie z OECD 492
Badanie przeznaczone jest dla wszystkich substancji, które podlegają rejestracji zgodnie z Rozporządzeniem REACH. Pozwala na rozróżnienie i zaklasyfikowanie badanej substancji jako „nie drażniącej” co odpowiada „No Category” wg GHS lub „żrącej/drażniącej” co odpowiada połączonej „Category 1” razem z „Category 2” wg GHS.
Badanie stopnia podrażnienia skóry
Przeznaczone jest dla wszystkich substancji (substancje czyste, mieszaniny, preparaty końcowe) w celu sprawdzenia oraz określenia ich potencjału lub stopnia podrażnienia skóry. Znajduje zastosowanie szczególnie dla nowych kosmetyków czy produktów higieny osobistej lub po zmianie formulacji i pozwala na uniknięcie uczestników badania na probantach, tym samym ograniczając ryzyko ich narażenia na substancje drażniące.
Badanie stopnia podrażnienia oka
Przeznaczone jest dla wszystkich substancji (substancje czyste, mieszaniny, preparaty końcowe) w celu sprawdzenia oraz określenia ich potencjału lub stopnia podrażnienia oka. Pozwala na przypisanie badanej próbce jednej z 4 kategorii stopnia podrażnienia jak również znajduje zastosowanie dla substancji dla których standardowy test Draize’a jest niewrażliwy w szczególności dla kosmetyków przeznaczonych do stosowania w okolicy oka.
Badanie przenikalności
Badanie polegające na sprawdzeniu za pomocą komór Franza obecności badanej próbki w płynie odbiorczym po przejściu przez model rekonstruowanego ludzkiego naskórka pełnej grubości. Badanie wykonywane we współpracy z Laboratorium Chromatografii i Spektrometrii Mas.
PCR, qPCR, RT-PCR
Metoda Łańcuchowej Reakcji Polimerazy (ang. Polymerase Chain Reaction) pozwala na powielanie konkretnych odcinków DNA in vitro. Real Time-PCR jest ilościową reakcją PCR (ang. quantitive PCR) umożliwia jednoczesne namnażanie wybranych fragmentów DNA oraz monitorowanie ilości produktów powstających podczas kolejnych cykli. Jagiellońskie Centrum Innowacji oferuje usługi w zakresie optymalizacji reakcji PCR oraz Real Time PCR metodą niespecyficzną SYBR Green lub metodą specyficzną przy użyciu komplementarnych sond oligonukleotydowych, których zasada opiera się na rezonansowym transferze energii fluorescencji (FRET) pomiędzy cząsteczką donora i wygaszacza. Dodatkowo oferujemy wykonywanie również RT-PCR (ang. reverse transcription PCR), w którym jako matrycę stosuje się RNA.
Technika PCR znajduje wiele zastosowań przede wszystkim w badaniach nad genomem, charakteryzowaniu ekspresji genów, klonowaniu genów i diagnostyce klinicznej.
Zespół
Kontakt w sprawie oferty:
K: +48 517 917 834
E: sales@jci.pl
Zaufali nam:
Noty aplikacyjne
The study of the influence of dmso on human fibroblasts proliferation in-vitro.
Więcej Zobacz wszystkie
In-vitro study of the cytotoxicity of cosmetic substances
Więcej Zobacz wszystkie







